分子の構造式を説明するモデル 電子配置を考えなくても、原子から何本手が出ているのかを考えれば、 あとはパズルを解くように組み合わせるだけで「構造式」を作ることができます。 正攻法で解けるならそれに越したことはありませんが、「電子配置何それ?」という生徒には 大きな効果を発揮すると思います(あまり喜ばしいことではありませんね汗)。 では、代表的な原子について手の本数をみていきます。 水素(H)=1本  酸素(O)=2本  窒素(N)=3本  炭素(C)=4本  他にはF(フッ素)やCl(塩素)も作りました。 手の本数は単に暗記させるのではなく、周期表から考えさせるようにしました。 では実際に原子を組み合わせて、分子を作ってみます。 手が余らないように組み合わせるのがポイント。 水素分子(H2)  互いに1本ずつ手を出して握手しています。 構造式は H−H となります。 酸素分子(O2)  2本の手で握手しています(二重結合)。 構造式は O=O 窒素分子(N2)  3本の手で握手しています(三重結合)。 構造式は N≡N このように、モデルを見ればひと目で構造式がわかるようになっています。 では、次に異なる種類の原子を組み合わせてみましょう。 水(H2O)  酸素(O)から出た2本の手に、それぞれ水素(H)が結合しています。 構造式は H−O−H 二酸化炭素(CO2)  炭素(C)から出た4本の手に、2つの酸素(O)が結合しています。 構造式は O=C=O アンモニア(NH3) 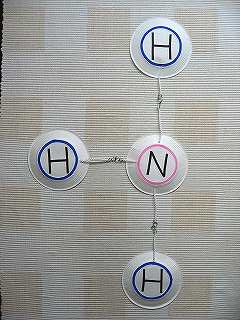 窒素(N)から出た3本の手に、それぞれ水素(H)が結合しています。 構造式は H−N−H | H メタン(CH4)  炭素(C)から出た4本の手に、それぞれ水素(H)が結合しています。 H | 構造式は H−C−H | H 同様に、C2H6やC3H8も組み立てていきます。 授業では私がいろいろな問題を出して、生徒にモデルを組み立ててもらいました。 授業のあとは皆、構造式を楽しんで書くようになってくれたので良かったなと思います。 最後にモデルの作り方をちょっと紹介。 なるべく安い材料ということで、本体には「紙皿」を使用しています。 紙皿にひもを取り付け、ひもの先端にS字フックをつけました。  ビニルひもの先端をライターであぶって、S字フックを引っ掛けています。 あとは実際に組み立てながら、ひもの長さを調節すれば完成です。 付記 DNA模型のページで紹介させていただいた「S.F.A1」のなかに、 「原子ブロックシステム」という素晴らしい教材が紹介されていますので、 そちらも参考にされると良いかと思います。 →教材一覧へ戻る |